藥智數(shù)據(jù)顯示,5月CDE受理1類創(chuàng)新藥141個品種,同比增加2%,其中IND申請128個品種,NDA申請13個品種。
1類創(chuàng)新藥NDA藥品名稱分別是索托克拉片、鹽酸吉卡昔替尼片、注射用重組巴曲酶、吡洛西利片、那米司特片、注射用康替唑胺鈉、苯甲酸安達替尼膠囊、GR2001注射液、通利腸溶膠囊、重組人源化單克隆抗體MIL62注射液、洛布替尼片、注射用STSP-0601、伊托法替布軟膏。
申報情況
5月CDE共受理新的藥品注冊申請1049個品種(受理號1352個),整體申報態(tài)勢穩(wěn)健。按藥品類型統(tǒng)計,化藥仍為主體,達627個品種;中藥235個品種;生物制品187個品種。按審評任務(wù)類型統(tǒng)計,受理新藥臨床試驗申請(以下簡稱IND)113個品種;新藥上市許可申請(以下簡稱NDA)33個品種;同名同方藥、仿制藥、生物類似藥上市許可申請(以下簡稱ANDA)254個品種;仿制藥質(zhì)量和療效一致性評價注冊申請(以下簡稱一致性評價申請)18個品種。
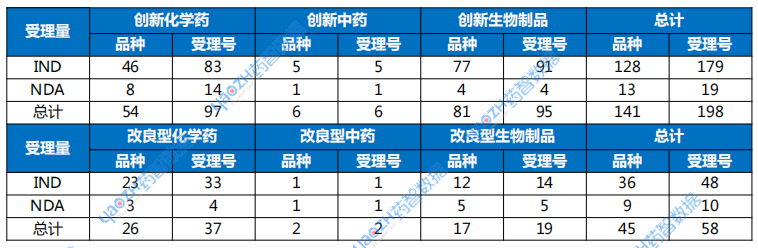
以注冊分類統(tǒng)計,1類創(chuàng)新藥受理141個品種。其中,IND申請128個品種,NDA申請13個品種。化藥創(chuàng)新藥上市申請8個品種;中藥創(chuàng)新藥上市申請1個品種;生物制品創(chuàng)新藥上市申請4個品種。
2類改良型新藥注冊申請受理45個品種,化藥申請26個品種,中藥申請2個品種,生物制品申請17個品種。
表1 2025年5月創(chuàng)新藥與改良型新藥注冊申請受理情況
中藥3類經(jīng)典名方注冊申請受理3個品種,為河北萬邦復(fù)臨藥業(yè)的苓桂術(shù)甘顆粒、四川光大制藥的完帶顆粒、瑞陽制藥的桃紅四物湯顆粒。
3類化學(xué)仿制藥注冊申請受理100個品種,驗證性臨床申請8個品種,上市申請92個品種。4類化學(xué)仿制藥受理175個品種。中藥同名同方藥受理1個品種,為健民藥業(yè)申報的鼻淵通竅顆粒。生物制品3.3類生物類似藥受理7個品種,其中預(yù)防用生物制品2個品種,治療用生物制品5個品種。
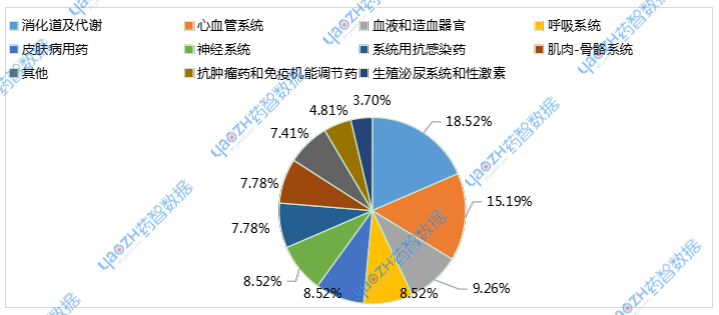
圖1 2025年5月化學(xué)仿制藥申報品種ATC分布情況
完成審批情況
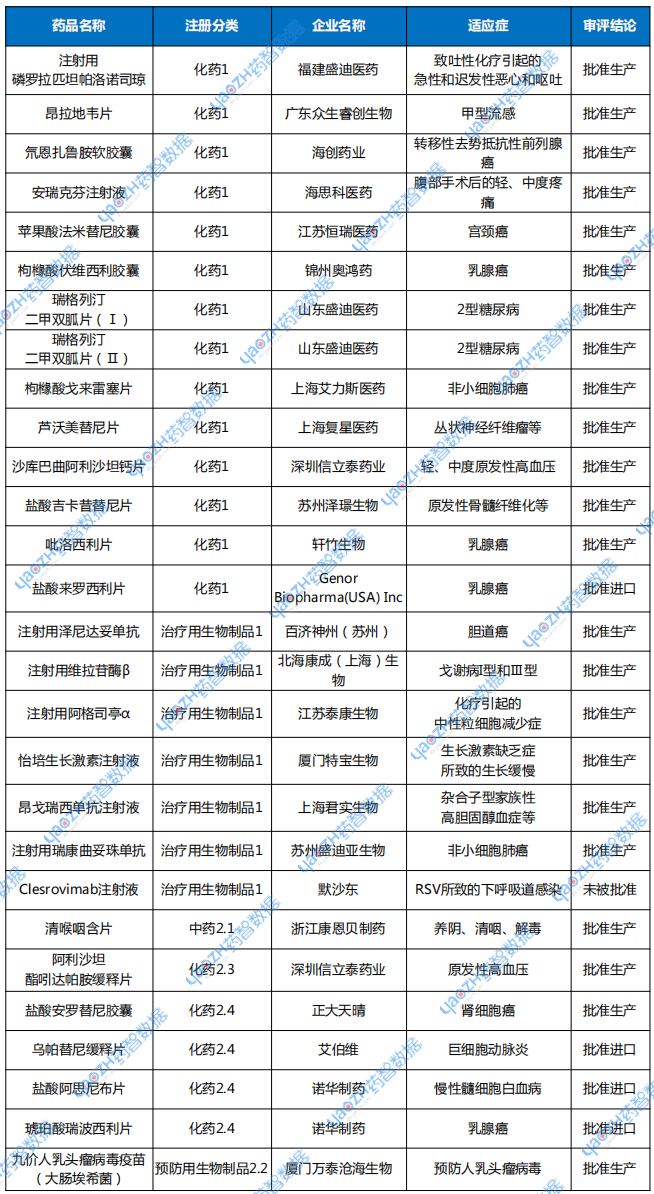
5月NMPA完成審批1008個品種(受理號1336個),其中化藥645個品種,中藥212個品種,生物制品150個品種。以審評任務(wù)類型統(tǒng)計,IND申請完成審批128個品種,NDA申請46個品種,ANDA申請294個品種,一致性評價品種33個品種。按藥智審評結(jié)論統(tǒng)計,批準(zhǔn)臨床192個品種,批準(zhǔn)生產(chǎn)296個品種,批準(zhǔn)進口17個品種,未被批準(zhǔn)61個品種。
以注冊分類統(tǒng)計,1類創(chuàng)新型新藥完成審批122個品種,IND申請完成審批103個品種,NDA申請21個品種,臨床批準(zhǔn)率為100%,上市批準(zhǔn)率為95%。2類改良型新藥完成審批37個品種,IND申請完成審批23個品種,NDA申請完成審批13個品種,批準(zhǔn)率均達100%。
3類化學(xué)仿制藥申請完成審批146個品種,批準(zhǔn)臨床14個品種,批準(zhǔn)生產(chǎn)122個品種,未被批準(zhǔn)10個品種。4類化學(xué)仿制藥申請完成審批159個品種,批準(zhǔn)臨床4個品種,批準(zhǔn)生產(chǎn)147個品種,未被批準(zhǔn)9個品種。中藥同名同方藥完成審批的4個品種(均為“開心散”),涉及四家企業(yè)(上海和黃、浙江康恩貝、安徽華潤金蟾、山東潤中),均未被批準(zhǔn)。3.3類生物制品生物類似藥5月未有完成審評品種。
表2 2025年5月新藥上市申請審評結(jié)論情況
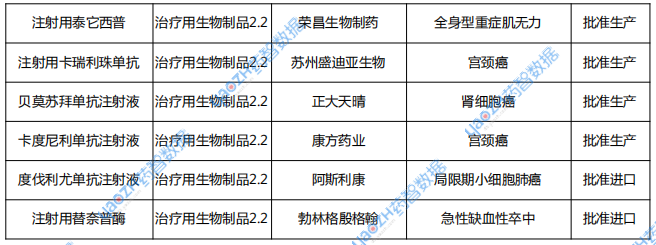
注:數(shù)據(jù)統(tǒng)計至2025年6月9日
優(yōu)先審評與突破性治療品種
5月CDE共將9個品種正式納入優(yōu)先審評名單,1個品種擬納入優(yōu)先審評。共計6個化藥品種,4個生物制品品種,中藥未有品種納入優(yōu)先審評。納入優(yōu)先審評理由涉及“納入突破性治療藥物程序”“附條件批準(zhǔn)”等。
突破性治療品種名單有6個品種,2個化藥,4個生物制品。涉及結(jié)直腸癌、肝細(xì)胞癌等適應(yīng)癥。
表3 2025年5月優(yōu)先審評與突破性治療品種名單
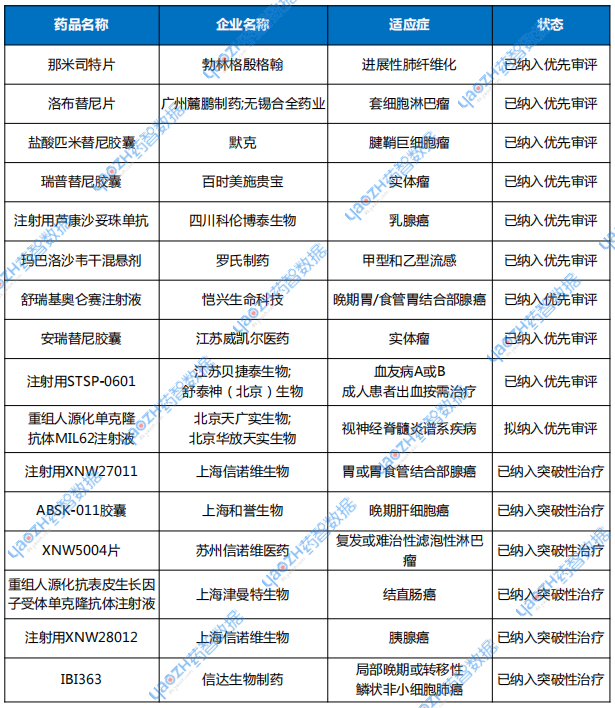
注:數(shù)據(jù)按公示日期進行統(tǒng)計







