在抗血栓藥物的璀璨星空中,有兩顆耀眼的明星不得不重點提及。其一是有著“全球最暢銷藥品”美譽的阿司匹林,全球年用量至今仍超1000億片,排列起來可繞地球 25 圈;其二便是阿哌沙班,上市以來銷售額不斷突破,穩坐小分子藥物銷量榜的頭把交椅。
而作為心血管疾病治療領域中的關鍵藥物類別,抗血栓藥物無論是在全球藥品銷量排行榜上,還是在臨床治療的實際需求中,其實都牢牢占據著首要位置,是心血管疾病治療不可或缺的“利器”。
如今,隨著全球人口老齡化趨勢愈發明顯,直接導致心血管疾病患者數量不斷攀升。同時,經濟水平的穩步提升也使得人們對健康的重視程度與日俱增,預防性抗凝在血栓栓塞性疾病高危人群中逐漸成為一種趨勢。
更關鍵的是,一代“神藥”阿哌沙班的專利懸崖正日益臨近,這不禁讓人思考:其時代逐漸落幕之后,屬于抗血栓藥物的傳奇還能否繼續?下一代抗凝王者又會是誰?
抗凝血
抗血栓領域的絕對主角
所謂抗血栓藥物,顧名思義就是一類能夠抑制血栓形成、促進血栓溶解或防止血栓擴展,從而預防和治療血栓栓塞性疾病的藥物。
根據其治療原理,大致可將抗血栓藥物分類為抗凝血類藥物、抗血小板類藥物、溶栓類藥物和血管擴張藥物。
其中溶栓藥物與血管擴張藥物存在臨床用藥局限(應用時間窗口短、臨時替代下肢深靜脈回流),因此理論上溶栓類藥物和血管擴張藥物并非抗血栓藥物的主體。
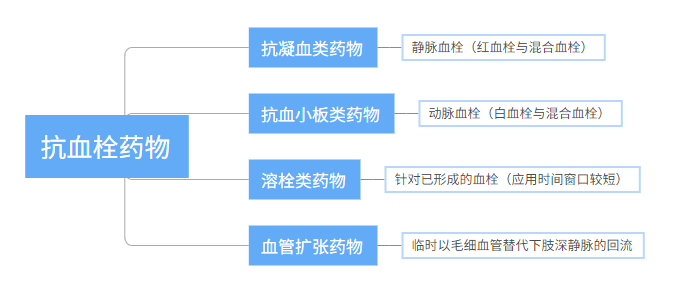
數據來源:公開數據整理
真正在抗血栓領域應用廣泛的是抗凝血類藥物與抗血小板類藥物兩者。
抗凝血藥物:主要針對靜脈血栓(紅血栓與混合血栓),因為靜脈血栓多由纖維蛋白和紅細胞構成,通常由血流緩慢或淤滯引起。
抗血小板藥物:主要針對動脈血栓(白血栓與混合血栓),因為動脈血栓主要由大量血小板和少量纖維蛋白構成,發生在血流較快的部位,主要由動脈粥樣硬化引起。
雖然兩者在抗血栓領域中的作用同樣顯著,但抗血小板藥物因其主要應用場景為動脈粥樣硬化性疾病(如冠心病、心肌梗死、腦卒中)的防治,其患者基數群體更大,但用藥周期卻相對更短(12月內);而抗凝血藥物的主要應用場景為房顫卒中預防、深靜脈血栓、肺栓塞及心臟瓣膜置換術后治療等,患者基數群體更低,但患者的長期用藥價值更高,部分患者更是存在終生抗凝治療的可能。
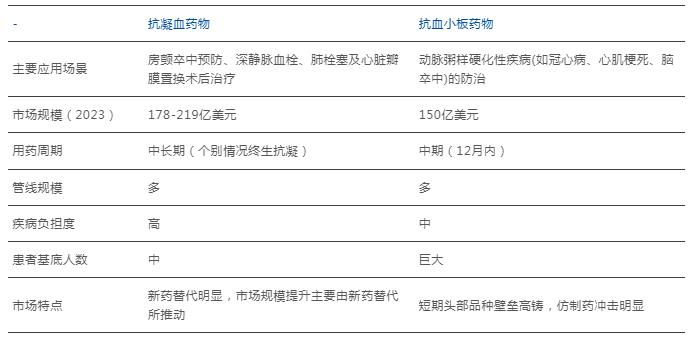
數據來源:公開數據,藥智咨詢整理
因此,綜合對比之下,抗凝血藥物的的市場規模反而更大,且增長速度也更快,更關鍵的是該領域歷經多種技術與產品的變革,新藥替代作用明顯,市場規模的增長與其新藥上市呈正相關性。
三大階段
抗血栓藥物發展
資料顯示,關于抗凝血藥物的探索最早可追溯到100余年前,彼時,德國學者Virchow提出的血管壁受損、血液流動減慢和血液成分改變的血栓形成三要素學說,并在之后的眾多領域學者共同努力下,血液凝固過程及其調控機制才得以被深入研究。
而從20世紀初發展至今,抗凝血藥物領域一共經歷了三個階段,分別是初步探索階段、快速發展階段與新藥奮起階段。
初步探索階段(1900—2000年):以?肝素?、?阿司匹林?和?華法林?的發現為標志性事件,逐步構建了現代抗凝治療的基石。
快速發展階段(2001-2012):受阿司匹林、華法林對抗凝領域的市場刺激,療效更好、安全性更強、綜合成本更低的第二代、第三代抗凝血藥成功進入市場,替代第一代抗血栓藥,比如利伐沙班、阿哌沙班等。
新藥奮起階段(2012年—2025年):盡管靶向抗凝血藥物的臨床應用愈發成熟,但其作用機制決定的出血風險仍在,因此大量新靶點、新機制的抗凝血藥物開始出現。
圖:抗凝血藥物階段發展的代表藥品與主導企業
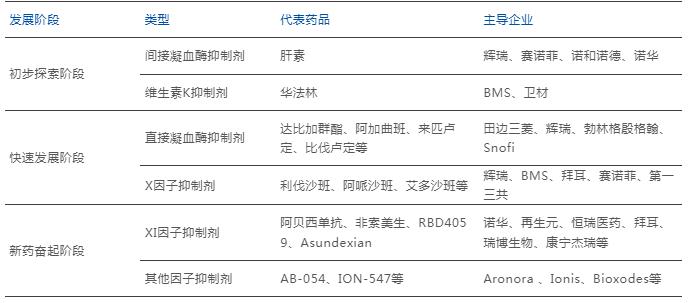
數據來源:公開數據,藥智咨詢整理
縱觀三個階段的新藥發展,其存在顯而易見的發展共性,即藥物的選擇性越來越強、有效性與安全性越來越高,患者順應性越來越被強調。并且發展過程中,輝瑞、BMS、拜耳、賽諾菲、GSK等MNC藥企的主導地位尤為明顯,可以說抗凝血藥物的發展方向正是MNC在背后推動,其任何布局都可能直接影響整個抗凝血領域的未來發展。
不過,隨著新型凝血因子Ⅺ抑制劑成為主要研究熱點,其技術主導的企業類型也逐漸出現了不分國產藥企的身影,且平均分布于各個技術類型,比如恒瑞的SHR-2004、瑞博生物的RBD-4059、海思科的EP-7041、康寧杰瑞的KN-060與靖因藥業的SRSD-107。
四大療法
抗凝血產品的階段性發展
據悉,在抗凝血領域,其主要作用機制均是圍繞凝血因子家族的抑制進行。
人體中一共有14種凝血因子,共同形成一個緊密且有序的聯絡網絡,當上游凝血因子被激活后,它們會像瀑布效應一般逐級激活下游因子,每經過一級,激活的凝血因子數量呈指數級增長,凝血效應亦隨之增強。這一過程被形象地稱為“凝血瀑布”。
最終,纖維蛋白原(Ⅰ因子)被激活并轉化為纖維蛋白網,捕獲血小板、紅細胞等成分,形成穩定的血栓。而在凝血因子中,其大多數并不直接參與血栓的形成,而是扮演傳遞信號或催化作用的角色,但其作用同樣至關重要。尤其是Ⅱ(凝血酶)和X因子,在藥物干預中占據關鍵地位。這也是為何早期抗凝血靶向藥都是圍繞Ⅱ和X因子推進的原因。
而從早期上市的肝素、華法林,到近20年以來的阿哌沙班、利伐沙班,抗凝血上市藥物的階段性發展主要圍繞四種藥物類型推進,即間接凝血酶抑制劑、維生素K抑制劑、直接凝血酶抑制劑與Xa因子抑制劑(下圖)。
全球部分抗凝血藥物的分類及已上市產品
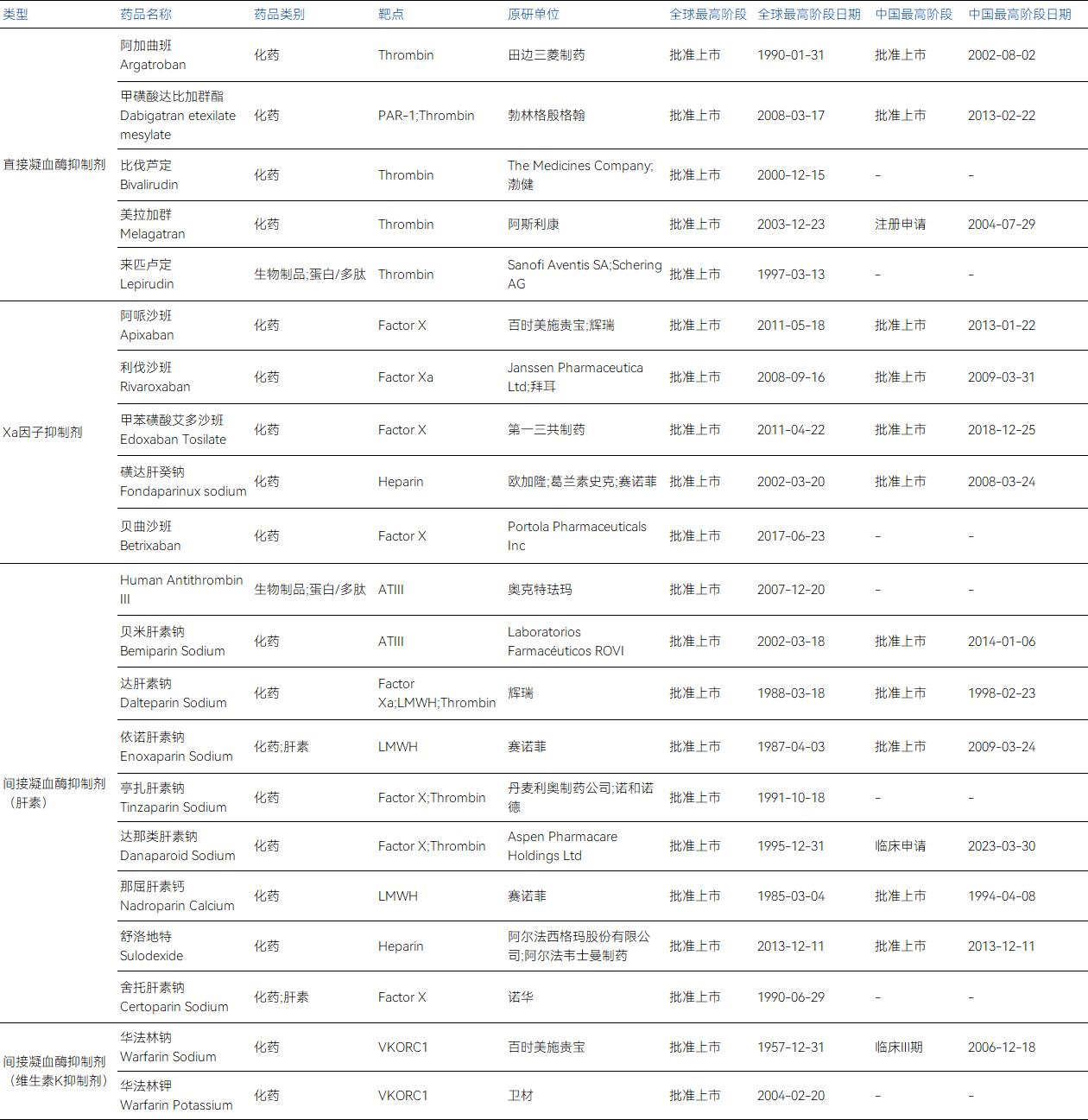
數據來源:藥智數據(點擊查看大圖)
間接凝血酶抑制劑
其主要通過與抗凝血酶(ATⅢ)的相互作用間接抑制Ⅱa、Ⅹa、Ⅸa、Ⅻa、Ⅺa的活性,發揮抗凝作用,不直接影響凝血酶,卻又能與抗凝血酶進行反應,讓抗凝血酶滅活凝血因子的速度大大加快,代表藥物為各種類型的肝素。
其臨床優勢在于抗凝血作用強、治療范圍廣,免疫原性風險低,缺點則由于其精準性不足(同時抑制多種凝血因子),整體抗凝反應不穩定,導致出血風險高,且長期應用還會影響免疫系統,增加感染的風險等。
維生素K拮抗劑
其主要通過抑制肝臟維生素K環氧化物還原酶,阻斷維生素K與其2,3-環氧化物(即維生素K環氧化物)之間的循環轉化,導致依賴維生素K的凝血因子Ⅱ、Ⅶ、Ⅸ、X無法完成羧化反應,進而抑制其生物活性,最終發揮抗凝作用,原則上其同樣是間接凝血酶抑制劑的一種,代表產品為各種類型的華法林。
其最大優勢在于可口服,適用于需要接受長期抗凝治療的患者,在靜脈血栓栓塞性疾病(VTE)、心房顫動、瓣膜病、人工瓣膜置換術以及心腔內血栓形成等血栓性疾病的預防和治療中發揮重要作用。然而其治療窗口窄,出血風險高,管理復雜的特點也使其成為抗凝治療的雙刃劍。
直接凝血酶抑制劑
其主要通過直接抑制凝血酶,阻止纖維蛋白原裂解為纖維蛋白,阻斷凝血瀑布的最后步驟及血栓形成,其中單價凝血酶抑制劑(達比加群酯,阿加曲班)可直接抑制凝血酶,二價凝血酶抑制劑(比伐盧定、重組水蛭素)直接抑制凝血酶的同時,還可以將凝血酶和纖維蛋白分離而達到抗凝作用。臨床上主要用于房顫卒中預防,急性冠脈綜合征、VTE的治療和預防(包括原發性和繼發性)。
代表藥物有達比加群酯、阿加曲班、來匹盧定、比伐盧定等。
臨床優勢上,相較間接凝血酶抑制劑,其既能夠滅活與纖維蛋白結合的凝血酶又能夠滅活血液中游離狀態的凝血酶,使其理論上的抗凝血效果更佳;同時由于其不與血漿蛋白結合,因此其生物利用度高、特異性更強,更關鍵的是副作用更低,極大地減少了出血風險與血小板減少癥(HIT)。但同時,其注射劑特性對于抗凝血治療領域不友好,依從性較差,用藥成本高,并伴隨明顯的消化不良并發癥。
Xa因子抑制劑
活化因子Xa作為一種絲氨酸蛋白酶,在凝血級聯反應中處于內外源凝血交匯地位,Xa 因子抑制劑可以使凝血瀑布的內源性和外源性途徑中斷,按是否依賴于ATⅢ因子可分為間接與直接抑制劑。間接Xa因子抑制劑需要ATⅢ因子作為輔助因子,不能抑制凝血酶原酶復合物結合的Xa因子;直接Xa因子抑制劑直接作用于Xa因子分子的活性中心,既抑制血漿中游離的Xa因子,也能抑制被凝血酶原酶復合物結合的Xa因子發揮抗凝作用。
代表藥品有利伐沙班、阿哌沙班和艾多沙班等。
臨床優勢方面,其靶點明確、與藥物食物相互作用小等優點,導致其被廣泛應用于血栓性疾病,并在多個指南中推薦優先級都高于傳統抗凝藥物。然后強如Xa因子抑制劑,其在出風風險控制方面仍有所不足。
整體而言,從間接凝血酶抑制劑到Xa因子抑制劑的發展中,抗凝血新藥發展特點明顯,即選擇性越來越強、有效性與安全性越來越高。而在此趨勢下,也預示著Xa因子抑制劑并非抗凝血藥物領域的理想載體,效果更好、出血風險更低、順應性更佳的抗凝藥物仍是血栓治療領域的熱點和趨勢。
XIa因子
抗凝血藥物的未來趨勢
正如前文所講,Xa因子抑制劑優異的有效性、可接受的安全性以及幾乎不存在的食物-藥物相互影響,使其成功替代傳統抗凝藥物(如華法林)成為臨床首選。
但隨著臨床對更理想抗凝藥物的不斷追求,越來越多研究正在評估靶向FXI或FXII對凝血級聯的潛在上游抑制是否有可能將血栓形成的機制從止血中分離出來,從而提供一種比DOAC更安全的抗凝方法。其中,Ⅺ凝血因子在相關流行病學調查中顯示,Ⅺ凝血因子缺陷者的患者的卒中發生率明顯較低,因此,其理論上具備在現有抗凝藥物基礎上進一步降低出血風險的可能。
因此,XIa因子抑制劑近年來逐漸成為可抗凝藥物的研發的主要方向之一。
據藥智數據顯示,目前全球在研抗凝血藥物共有34款(活躍),其中XIa因子抑制劑就超過20款,占所有在研抗凝藥管線的60%以上。足見其在抗凝血新藥研究的中超然地位。
并且,針對同一靶點,眾多Ⅺa因子抑制劑在不同需求層面,發展出了不同的設計方案,比如XIa因子單克隆抗體、XIa因子小核酸藥物和XIa因子小分子抑制劑。
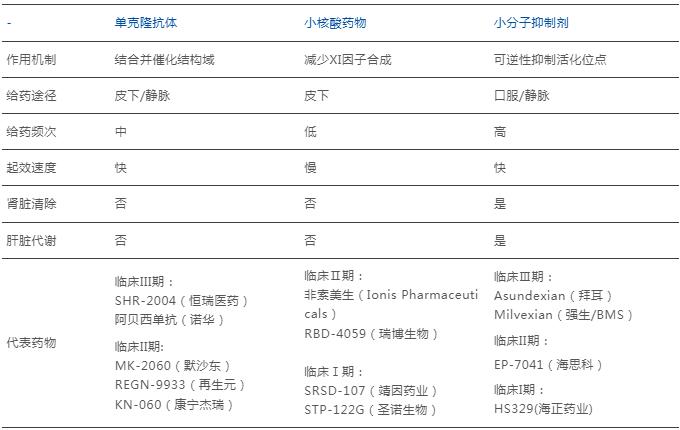
數據來源:公開數據,藥智數據,藥智咨詢整理
XIa因子單克隆抗體-阿貝西單抗
阿貝西單抗是諾華一款靶向凝血因子Ⅺ(FXI)的人源化單克隆抗體,可選擇性結合FXI和凝血因子XIa(FXIa),阻礙凝血因子XIIa(FXIIa)對FXI的激活,從而阻斷內源性凝血途徑的級聯反應過程,發揮抗凝作用。同時,該藥還是全球Ⅺ因子單抗中臨床進展最快的產品。
2025年初,其一項比較阿貝西單抗與利伐沙班的有效性與安全性研究(AZALEA-TIMI 71)的實驗中,結果顯示,用藥3月之后,有效性方面,150mg劑量阿貝西單抗組患者的游離 Ⅺ 因子平均降低了99%,90 mg劑量下降了97%。安全性方面,與利伐沙班比,阿貝西單抗150 mg組降低出血風險62%,90mg組降低69%,出血事件減少幅度遠大于預期,因此試驗提前終止。
很明顯,以阿貝西單抗為代表的Ⅺ因子單抗較Xa因子抑制劑,至少安全性方面具備明顯優勢,充分滿足了其臨床迫切需求。
XIa因子化藥-Asundexian
作為目前XIa抑制劑中最主要的技術類型,小分子XIa靶向抑制劑能夠快速擴散穿過細胞膜到達細胞內的作用位點,迅速發揮作用,而除此之外,小分子藥物還具備口服與腎臟清除壓力等特點。
目前,全球活躍在研小分子XIa靶向藥領域,尚無任何一款新藥成功上市,臨床進度最快的當數Asundexian(拜耳)與Milvexian(強生/BMS)。
以Asundexian為例,其作為拜耳一種口服的化學合成小分子,能夠直接、有效、可逆地抑制Xia因子。該藥的完全生物利用度不受片劑配方、胃pH值或食物的影響。在一項之前的2期臨床研究中,其結果顯示,在房顫患者中Asundexian的出血風險(根據ISTH標準的大出血或臨床相關非大出血)低于阿哌沙班。
PACIFIC-STROKE試驗在1800名急性非心源性缺血性卒中患者中評估了Asundexian用于缺血性卒中二級預防的作用,與安慰劑相比,Asundexian未減少隱匿性腦梗死或缺血性卒中復合終點發生率,也不增加大出血或臨床相關非大出血、所有出血、出血轉化的風險。
OCEANIC-AF試驗將在約15000名房顫患者中評估Asundexian與阿哌沙班的療效和安全性。OCEANIC-AMI 3期試驗將評估在雙聯抗血小板治療基礎上使用Asundexian對心血管事件和死亡風險的影響。
XIa因子小核酸藥物-RBD4059/SRSD-107
鑒于XIa抑制劑對比Xa因子抑制劑具有更有效的抑制效果,且出血風險更低,部分企業試圖在XIa單抗上進一步優化其順應性局限性,siRNA就是其中最被寄予厚望的療法。
RBD4059作為瑞博生物基于其肝靶向技術平臺開發的GalNac偶聯siRNA藥物,通過抑制凝血因子Ⅺ(FXI)和阻斷內源性凝血途徑的激活,從而實現其抗凝血/抗血栓的作用。已有臨床Ι期結果顯示,RBD4059呈現出劑量依賴性、可預測的藥代動力學特性,以及顯著的(>90%)和持久的FXI活性和蛋白降低效果;同時,在安全性和耐受性方面達到主要終點,在研究的劑量范圍內未發現不良安全信號,顯示出良好的安全性。
SRSD107作為靖因藥業一款雙鏈小干擾核酸(siRNA)藥物,旨在選擇性抑制凝血因子Ⅺ(FXI),通過靶向FXI,SRSD107有望在降低血栓事件發生的同時,顯著減少出血風險,展現出有別于凝血因子X活性(FXa)抑制劑的治療優勢。在其臨床一期試驗結果中,SRSD107安全性和耐受性良好,并觀察到藥效生物標志物相較基線的顯著變化。在最高給藥劑量下,FXI抗原及FXI活性的最大降幅超過90%,aPTT增幅超過100%(即aPTT 比值> 2.0)。單次給藥后的藥效效應持久,維持FXI抗原及FXI活性近90%抑制狀態時長超16周。
很明顯,XIa靶向siRNA療法除了常規上更強效的抑制作用外,其與單抗最大的區別特性在于其具備長效優勢,最高半年一次的用藥頻率極大地改善了患者依從性,并降低藥物相互作用風險。
很明顯,三種技術類型各有優勢,也各有其局限性存在,以目前的試驗結果尚無法判斷其未來的最終走向,唯有三個領域在成藥性逐一驗證之后的頭對頭數據,才真正具有參考意義,不過粗略來看,以抗凝血藥物的主要應用場景,或許小核酸與小分子口服藥的優勢相對較大。
小結
綜上所述,抗血栓藥物的發展歷經百余年探索,從最初以肝素、華法林為代表的傳統藥物,到如今以XIa因子抑制劑為代表的新一代創新療法,其研發路徑始終圍繞“選擇性增強、有效性提升、安全性優化”三大核心目標推進。
而以目前全球抗凝血藥物的研發趨勢來看,市場已形成以Xa因子抑制劑為主導、XIa因子抑制劑為突破口的競爭格局,其中XIa因子抑制劑憑借其理論上更低的出血風險和更廣泛的適應癥潛力,正成為跨國藥企(MNC)與生物技術公司競相布局的熱點領域。
同時,在XIa因子抑制劑的技術方向發展上,總體呈現出三種優勢不同的技術方向:
單克隆抗體(如阿貝西單抗)通過精準阻斷內源性凝血途徑展現卓越安全性。
小分子抑制劑(如Asundexian)憑借口服便利性與快速起效優勢推進大規模臨床驗證。
小核酸藥物(如RBD4059、SRSD107)則依托長效作用機制與肝靶向遞送技術,試圖在降低給藥頻次的同時突破傳統藥物的療效-安全性平衡。
總而言之,如今的抗凝血藥物很明顯已進入?精準化、長效化、安全化發展的?新階段,未來十年,領域更是將呈現“多技術并行、差異化適應癥覆蓋”的競爭趨勢。







